
| 不整脈について > | カテーテルアブレーション > |
| 診療実績 > | 植え込み型ディバイス > |
| 医師紹介 > | 外来診療・お問い合わせ > |
不整脈について
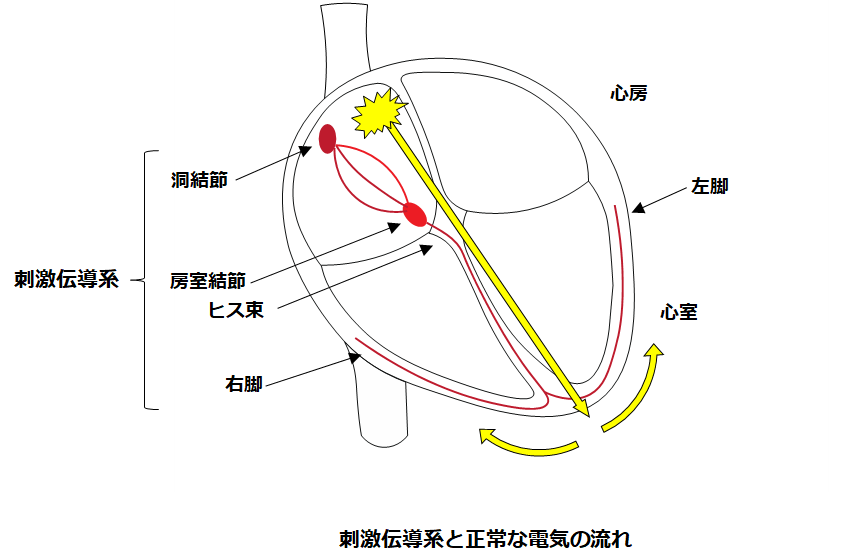
ヒトの心臓の中には電気信号が流れており、その電気信号が心臓の筋細胞に伝わることに よって収縮運動が起こります。心臓内には洞結節(洞房結節)という人間が本来持っているペース メーカ細胞群があり、電気信号はそこから1分間に60〜100回ほど発生しています。
その電気信号が心臓全体に流れるための電線を刺激伝導系といい、電気信号が刺激伝導系を伝わり心臓が収縮すると、全身に血液が送られ脈拍として触れることができます。
心拍数が100回/分を超える場合を頻脈といい、60回/分未満を徐脈といいます。また 不規則性に、単発または連発で拍動する不整脈を期外収縮といいます。頻脈は動悸や息切れ、 胸の不快感・失神などを引き起こし、徐脈はめまい・倦怠感・失神などを引き起こします。 期外収縮は無症状のことも多いですが、「脈がとぶ」症状を感じることもあります。
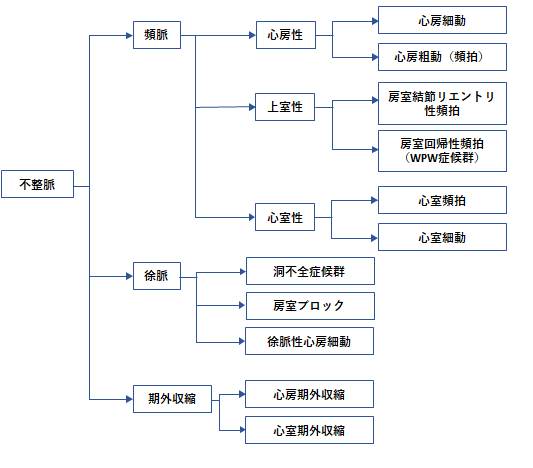
不整脈の分類
不整脈の治療
頻脈に対する治療は①カテーテルアブレーション(経皮的心筋焼灼術)、②薬物治療、 ③電気的除細動(植え込み型除細動器を含む)となります。年齢や症状に応じて治療を行うかどうか決定します。難治が予想される場合は、上記3つを組み合わせて治療することも あります。

期外収縮に対する治療は①カテーテルアブレーション(経皮的心筋焼灼術)、②薬物治療となります。頻度や症状に応じて治療を行うかどうか決定します。
それぞれの不整脈について
心房細動
心房細動は不整脈の中で最も多い疾患で、発作時は心臓の“心房”と呼ばれる部分が 痙攣したような動きになります。心臓にもともと病気がない人でも年齢が上がるにつれて多くみられるようになり、様々な症状や病気を引き起こします。初めの頃は 発作と停止を繰り返す発作性心房細動、発作が1週間以上持続すると持続性心房細動、1年以上持続すると長期持続性心房細動という病名になり、持続時間が長いほど治療 が困難になると言われています。
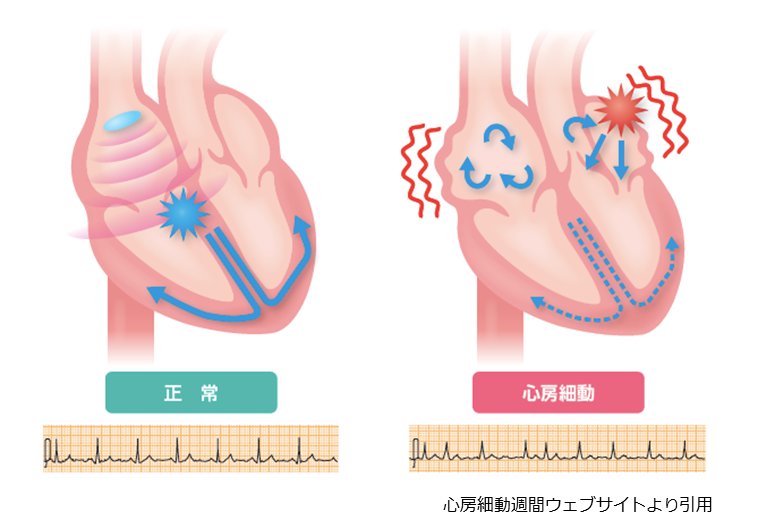


心房細動の初期は発作時に心拍数が上昇してしまうため動悸症状を感じやすいと 言われています。他にも運動した時に息切れ症状を感じてしまう場合もあれば、じっとしている時でも胸の不快感を自覚することがあります。心房細動が慢性化した場合や、 また慢性化していなくても約40%の方は動悸などの症状を感じにくいと言われています(※)。しかしそうした症状がなくても以下のような深刻な合併症をきたす場合もあり、 注意が必要です。
心房細動の症状② 脳梗塞・全身性塞栓症
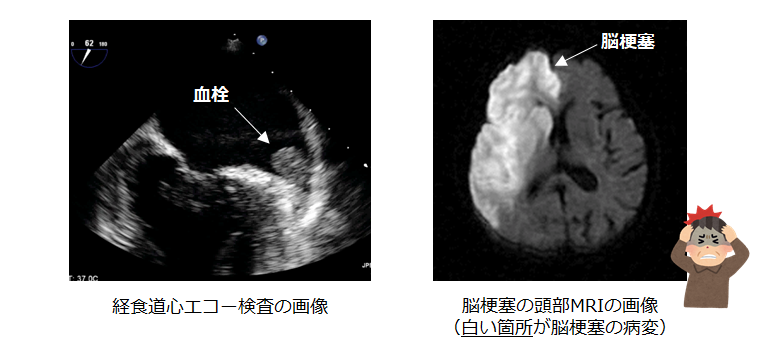
心臓の中における血流が滞ることによって血栓(血のかたまり)が形成されます。
それが全身に飛ぶことによって様々な塞栓症を引き起こします。特に重大なのが脳梗塞で、もともと血圧が高い方や糖尿病をお持ちの方、75歳以上の方が発症しやすいと言われています(※)。また心房細動が原因で発症する脳梗塞は他の原因よりも重症化することが 知られています。(下記はいずれも当院実施の検査画像)
※ Ann Intern Med 2009;151:297–305
心房細動の症状③ うっ血性心不全
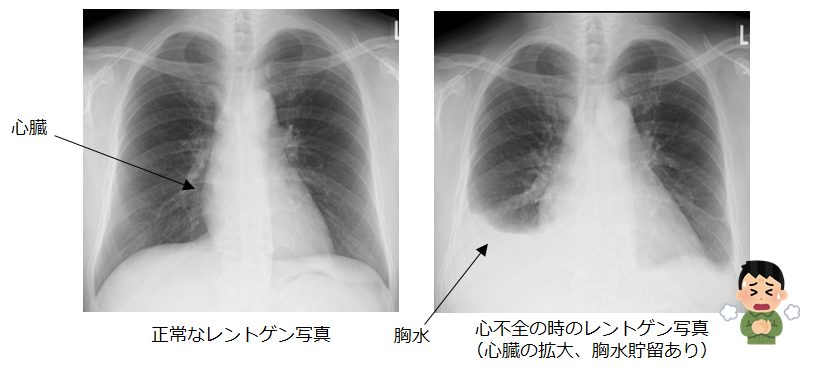
心拍数が非常に速い心房細動を発症したり、また心房細動を長い年月放置しておくと心臓の動きが悪くなってくることがあります。心臓は体の中で「血液ポンプ」として働いているのでその動きが悪くなると血液の循環が滞り、足がむくんだり肺に水が溜まる心不全の症状が出現することがあります。

ごく小さな脳梗塞は無症状ですが、それを長年積み重ねると認知症になりやすくなるという報告があります(※1)。また介護が必要になる疾患としては認知症が最も多く、次いで脳梗塞をはじめとした脳血管疾患が多いとされています(※2)。
よって心房細動により将来的に生活の質が低下する可能性があり、注意が必要です。
※1. JAMA Neurol.2015 Nov;72(11):1288-94.
※2. 厚生労働省HP国民健康基礎調査より
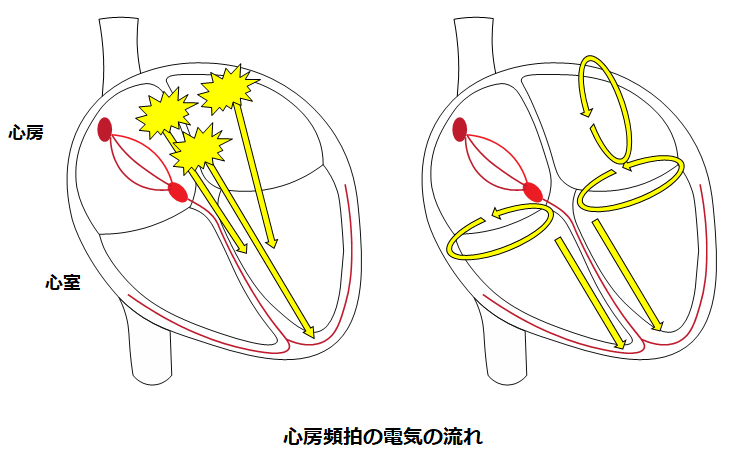
心房粗動(頻拍)
心房粗動は色々なタイプがあり、もともと心臓に病気がない人でも起こるものもあれば、心臓手術後に起こるもの、また心房細動に対するカテーテルアブレーション後に起きやすいものもあります。心房細動と同じく、“心房”と呼ばれる部分が痙攣したような動きになります。心房細動に準じて治療を行います。
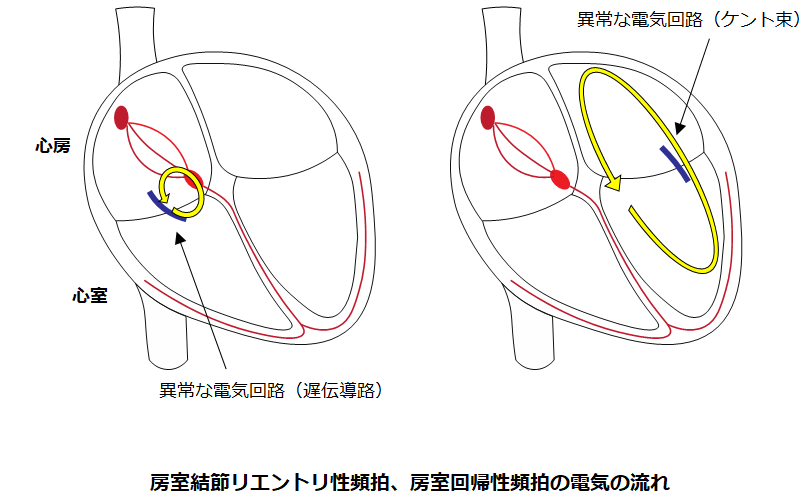
房室結節リエントリ性頻拍、房室回帰性頻拍
房室結節リエントリ性頻拍と房室回帰性頻拍は、「異常な電気回路」を介して心臓の中で電気興奮が旋回する頻脈で、激しい動悸症状を自覚する場合があります。
カテーテルアブレーションが唯一の根治治療となります。タイプによって様々ですが、カテーテルアブレーションにより概ね90%以上の成功率が期待できます。
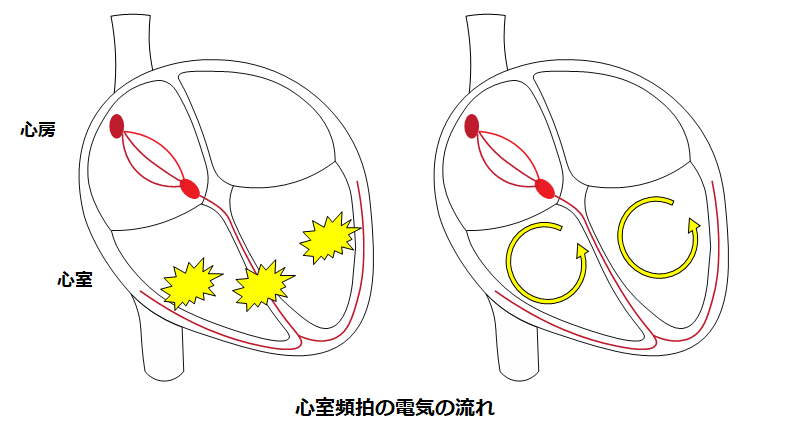
心室頻拍
心臓の中の“心室”と呼ばれる部分から発生する不整脈です。心筋梗塞や心筋症といった病気が原因で発症することもありますが、特に心臓の病気がなくても発症するケースもあります。電気信号の流れ方も含めて様々なパターンがありますが、突然死の可能性があるため、カテーテルアブレーションだけでなく、植え込み型除細動器が必要になる場合があります。
心室細動
心臓の中の“心室”と呼ばれる部分から発生する不整脈です。心筋梗塞が原因で発症する場合もあります。突然死の原因となります。カテーテルアブレーションは特殊なケースを除いて無効であり、植え込み型除細動器と薬物治療で再発を予防します。
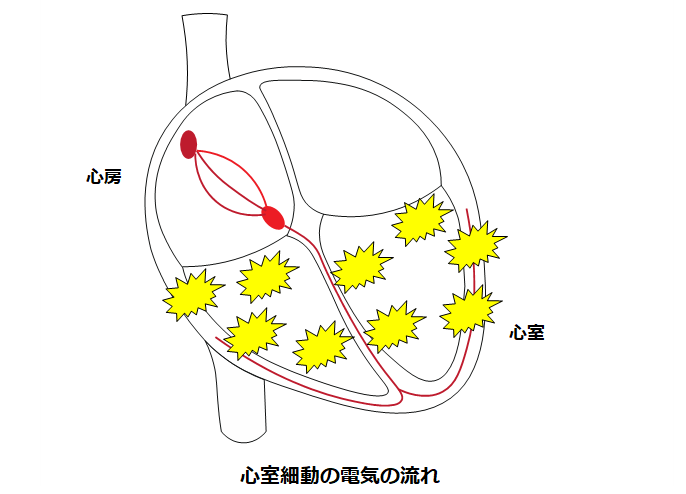
心房・心室期外収縮
心房または心室から不規則なタイミングで電気信号が発生します。特に心臓の病気がなくても起こります。数が少なければ治療の必要はありません。症状や頻度によって治療を行うかどうか決定します。
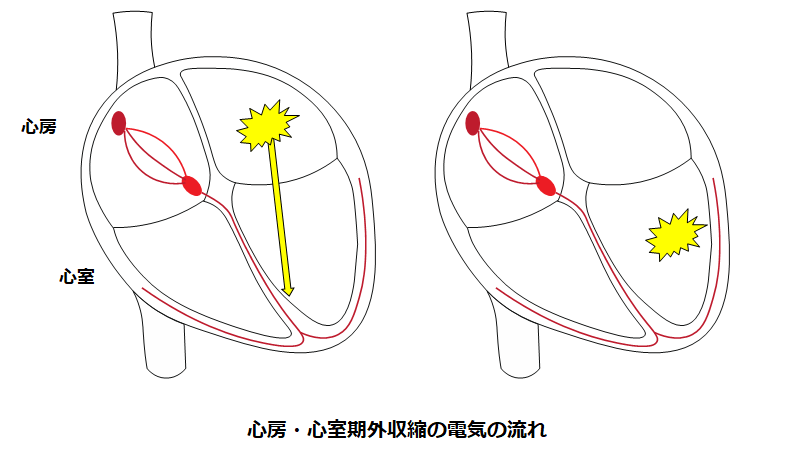
洞不全症候群
洞結節(洞房結節)からの電気信号の数が減ることによって心拍数が減少します。年齢とともに発生する頻度が増えます。原則としてペースメーカー植え込みが必要となりますが、心房細動と合併するタイプはカテーテルアブレーションを行うことで改善することもあります。治療方針は症状や年齢などを考慮して決定します。
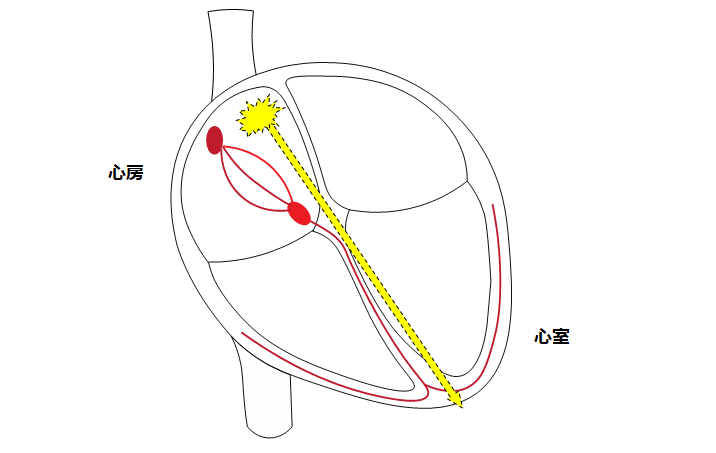
房室ブロック
刺激伝導系が断線し、電気信号が正しく心室に伝わらないことによって心拍数が減少します。
心筋梗塞に合併し、一時的に出現することもありますが、多くは年齢とともに頻度が増え、不可逆性です。突然死の原因になることもありますのでめまいや失神、息切れや倦怠感などの症状があれば速やかなペースメーカー植え込みが必要となります。
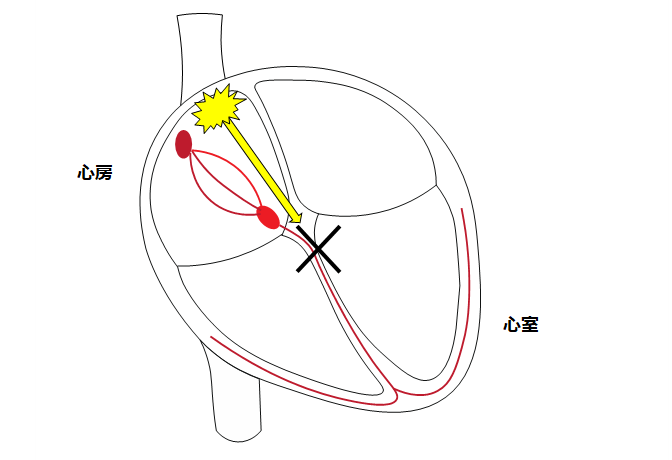
徐脈性心房細動
当初は頻脈だった心房細動が時間の経過とともに徐脈に変化することもあります。刺激伝導系の断線や心房の電気活動が低下していることなどが原因と考えられています。めまいや息切れ、倦怠感などの症状があればペースメーカー植え込みの適応となります。
カテーテルアブレーション
高周波を発するカテーテルを足の付け根(鼠径部)から挿入して心臓の中に進めます。
不整脈の原因となっている箇所に対して高周波による焼灼(アブレーション)を行い不整脈を根治させます。症例によって右首や右手首からカテーテルを挿入することもあります。
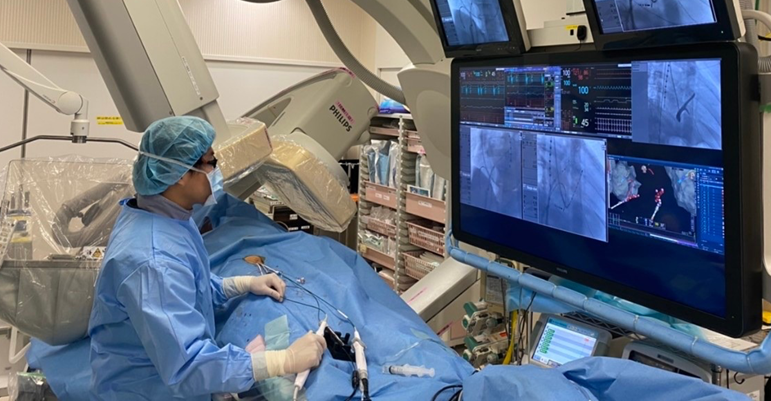
カテーテルアブレーションの術中風景
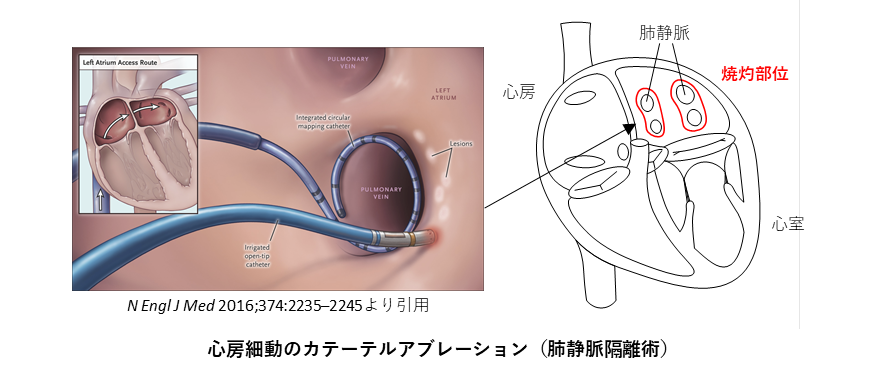
心房細動のカテーテルアブレーション
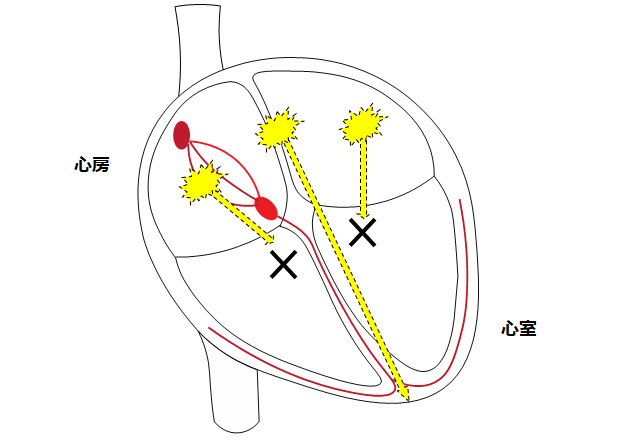
発作性心房細動の約90%が左心房にある肺静脈が原因といわれています。ここから異常な電気信号(トリガー)が発生し、心房内に伝わることで心房細動が引き起こされると考えられており、心房細動アブレーションはこの電気信号が心房内に伝わってこないように、肺静脈入り口の周囲を通電・焼灼して電気的な交通を遮断します(上図)。この手術は肺静脈隔離術といいます。
また心房細動は肺静脈のみならず、右心房にある上大静脈が原因で発症するものもあれば、頻度は少ないものの心房内からの異常信号で発症することもあります。その場合、追加の治療が必要になります。
心房細動が発症するメカニズムは研究により明らかとなりましたが、一旦発症した心房細動がなぜ持続するのかについては完全には解明されていません。そのため持続性心房細動に対するカテーテルアブレーションの治療成績は、発作性心房細動に対するそれと比較し低いと言われています。持続性心房細動に対して肺静脈隔離術だけ行なっても術後1年以内に 40%程度再発してしまうというデータもあります(※)。そのため持続性心房細動に対しては各施設が色々な工夫を行い治療しているのが現状です。当院では発作性心房細動に対しても、以下のような工夫を行いアブレーションを行なっています。
※N Engl J Med 2015;372:1812-1822
① 上大静脈を含む非肺静脈起源のトリガーに対するアブレーション
上記の通り、心房細動は肺静脈以外からの異常な電気信号(トリガー)でも発生します。そのため当院では肺静脈隔離(術)に加えて上大静脈に対するアブレーションも積極的に行なっています。また心臓内から発生するトリガーを同定するために薬剤を使って誘発しアブレーションを行なっています。これらの追加治療を行うことで成功率を少しでも高めることができるよう工夫しています。
② 全身麻酔と局所麻酔の併用
局所麻酔のみでアブレーションを行うことも可能ですが、当院では局所麻酔と全身麻酔を併用し、術中の苦痛を可能な限り軽減するよう努めています。また原則、尿道バルーンの挿入は行いません。また鼠径部をはじめとしたカテーテル挿入部は縫合して止血しますので術後の安静時間も短く、麻酔が覚めた段階で動くことができます。
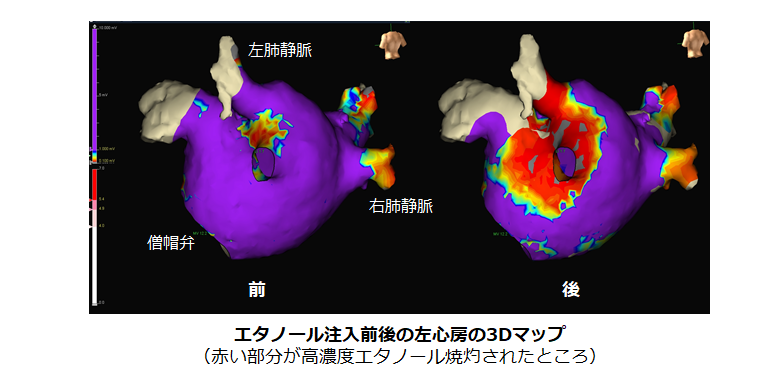
③ 高濃度エタノールを併用した線状焼灼
上で述べた通り、持続性心房細動は肺静脈隔離術だけでは再発してしまうことが多いため、追加の治療が必要となる場合があります。当院では左心房内に“線を引く”ような形で焼灼する左房内線状焼灼(下図)を積極的に行なっています。これは心房細動のトリガーに対する治療ではなく、心房細動を自然停止しやすくするための治療です。線状に焼灼した部分で電気信号の流れが遮断され、心房細動が停止しやすくなると考えられています。医学的根拠の確立はまだ途上ですが、成功率を少しでも高めるために当院ではこの方法を採用しています。
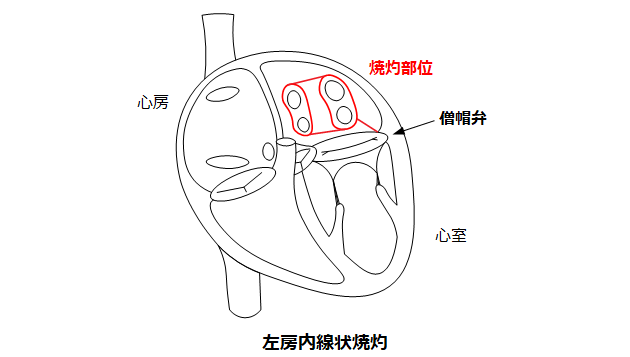
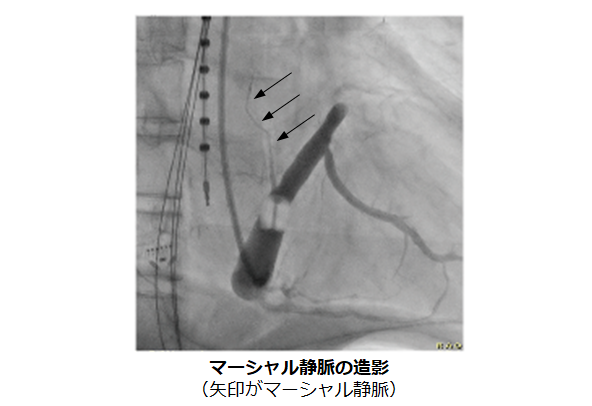
問題点として、心臓の筋肉が厚い僧帽弁輪においては高周波の焼灼だけだと効果が不十分な場合があります。不十分な焼灼は逆に他の不整脈(心房頻拍)の原因となってしまうことがありますので、それを解決するために当院では高濃度エタノールを併用してアブレーションを行います。
マーシャル静脈という僧帽弁輪付近にある細い血管に高濃度エタノールを注入することで心房を焼灼します。これを行うことで僧帽弁輪アブレーションの成功率が飛躍的に向上することが当院のデータでも示されています(※1)。エタノールによる焼灼は僧帽弁輪以外にも肺静脈や心臓周囲の自律神経をも焼灼すること、術後に心房頻拍が発症することも抑制する効果も示されており、心房細動アブレーションの成功率向上に寄与することが期待されています。
※1 J Cardiovasc Electrophysiol. 2021;32:2116-2126
心房細動以外のカテーテルアブレーション
当院では全てのカテーテルアブレーションも原則、全身麻酔で行っています。心房細動のアブレーションと異なり短時間で終了することも多いため、原則、尿道バルーンは挿入しません。また穿刺部は縫合して止血するので術後は比較的早い段階で動くことができます。
カテーテルアブレーション治療を受ける方のスケジュール
カテーテルアブレーションの入院期間は原則3泊4日となります。

退院後の生活
 退院日より入浴は可能です。散歩などの歩行も問題ありませんが、自動車運転は退院後1週間は控えて下さい。ジョギングなどの心拍数が上昇する運動は2週間程度避けて下さい。
退院日より入浴は可能です。散歩などの歩行も問題ありませんが、自動車運転は退院後1週間は控えて下さい。ジョギングなどの心拍数が上昇する運動は2週間程度避けて下さい。また飲酒は不整脈を起こしやすくするため退院してから1ヶ月程度は控えて下さい。
仕事の復帰は業種や業務内容によって変わりますので入院中に主治医までお尋ね下さい。
カテーテルアブレーション後に起こりうる合併症
 心房細動が持続することにより血液の流れが滞り、心臓内に血の塊(血栓)が形成されることがあります。またカテーテルアブレーションで火傷した部分に血栓が形成されやすいことが知られており、術後も抗凝固薬の内服が必要になります。完全に予防することは難しく、0.3%程度の確率で起こりうるとされています。当院での発症確率は0.1%程度です。
心房細動が持続することにより血液の流れが滞り、心臓内に血の塊(血栓)が形成されることがあります。またカテーテルアブレーションで火傷した部分に血栓が形成されやすいことが知られており、術後も抗凝固薬の内服が必要になります。完全に予防することは難しく、0.3%程度の確率で起こりうるとされています。当院での発症確率は0.1%程度です。
 心房細動から心不全を発症するケースが非常に多いとされています。アブレーション後に心不全の兆候があれば、利尿薬などを用いて心不全治療を強化します。
心房細動から心不全を発症するケースが非常に多いとされています。アブレーション後に心不全の兆候があれば、利尿薬などを用いて心不全治療を強化します。
③ 血管損傷
頻度は少ないものの、カテーテルを挿入した静脈の隣にある動脈が傷つけられることがあります。術後、歩行中に痛みを感じる場合はすぐに相談して下さい。発症する頻度は 0.2%程度です。
④ 食道迷走神経障害
食道と並走している迷走神経が火傷することにより胃や腸の動きが一時的に悪くなることが あります。発症頻度は0.1%程度です。
⑤ 徐脈性不整脈
心拍数が異常に増加する心房細動などの頻脈性不整脈がある一方、心拍数が異常に低下する徐脈性不整脈が存在します。徐脈性不整脈と診断された患者の40〜70%に心房細動が併存している※といった報告があり、比較的まれではありますがカテーテルアブレーション術後にめまいや失神を発症することがあります。これは今まで心房細動に隠れていた徐脈性不整脈が、心房細動が治ることによって表に出てくるためと考えられており、場合によってはペースメーカ植え込みが必要になってくることもあります。
カテーテルアブレーションの術前に徐脈性不整脈の存在を予想することは難しいと考えられており、もし術後に徐脈になった場合は症状や検査結果をふまえてペースメーカの必要性を検討していくことになりますのであらかじめご承知おき下さい。
※N Engl J Med. 2002; 346:1854–1862 J Cardiovasc Electrophysiol. 2002; 13:542–547
初回治療後に心房細動が再発してしまった患者さんへ
初回治療後に再発してしまう主な理由としては、
① 初回治療時の焼灼が不十分だった。
② 肺静脈以外に心房細動の原因となるトリガーを有していた。
③ 時間の経過とともに、心臓内に新たに不整脈の原因となる基質が形成された。
①の場合
初回治療時の焼灼が不十分であっても、焼灼直後は判別しにくい場合があります。しばらくすると焼灼した部分が元通りになってしまうことで、伝導性が回復し心房細動が再発してしまうことがあります。

②の場合
上で述べたように発作性心房細動の90%以上が左心房にある肺静脈が原因と言われています。
他にも数%程度の割合で上大静脈が原因となることもあり、当院では肺静脈と上大静脈に対してアプローチをすることで成功率を向上させていますが稀に肺静脈と上大静脈以外が原因となることがあります。これは心臓内から異常な電気信号(トリガー)が発生するためで、肺静脈同様心房細動へと進展することがあります。初回アブレーション時から薬剤を使用して誘発してはいるものの、標的となる部位が絞りにくいためアブレーションの成功率が比較的低いと 考えられています。
③の場合
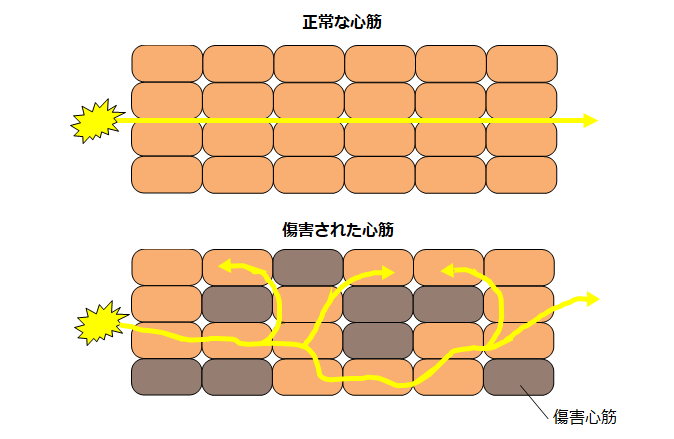
正常な心筋では、電気信号がスムーズに通過していきますが、傷害された心筋は電気信号の流れが複雑化するようになります。時間の経過と共に心筋が傷害されていくと下記のように電気が局所で旋回しやすくなり、不整脈が起きやすくなると考えられています。
2回目のカテーテルアブレーションはこれらを踏まえて治療を行うため、
根治率は初回治療のみと比べて上昇します。
植え込み型デバイス(ペースメーカなど)
洞不全症候群や房室ブロックなどの徐脈に対する治療としてペースメーカ植え込みを行います。ペースメーカ本体より微弱な電気を流し、心臓を60回/分以上で動かすことによってめまい症状や失神を防ぐことができます。
ペースメーカは左前胸部に植え込みます。皮膚を4〜5cmほど切開し本体を植え込みます。
通常2本のリード線を心房および心室内に留置して本体に接続します。(下図)またリード線の留置を必要としないリードレスペースメーカの植え込みも行なっています。徐脈の種類によって、また併存疾患などで適応を決定します。
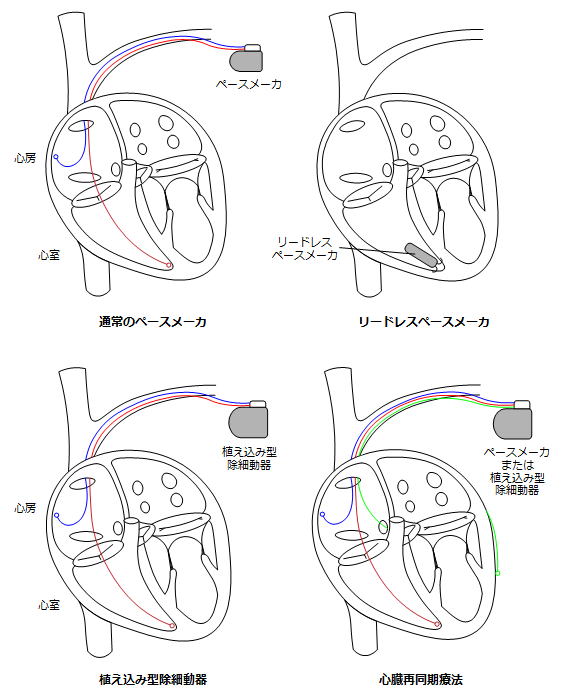
致死性の頻脈に対しては発作時に電気的除細動を行うために植え込み型除細動器(ICD)の植え込み手術を行うことがあります。ペースメーカと同様に本体と1本または2本のリード線を挿入し心臓内に留置します。また心不全に対する治療として心臓再同期療法(CRT)を行うことがあります。この場合、心室に2本リード線を留置するためリード線は合計3本になります。これらの手術は全て局所麻酔で行われ、ペースメーカと植え込み型除細動器の手術時間は概ね1時間程度、心臓再同期療法は2〜3時間程度となっています。ペース メーカ・植え込み型除細動器の新規植え込みでは3泊4日、交換は2泊3日で行います。
心臓再同期療法は新規植え込みで1週間、交換は2泊3日で行います。
退院後の生活
退院1週間後、創部が完全に治癒したら入浴が可能です。植え込み側の腕を上げることはほとんど問題ありませんが水泳やゴルフなどの腕を回す運動は2ヶ月程度控えて頂いています。
当院ではペースメーカは1年ごと、植え込み型除細動器および心臓再同期療法後は半年ごとにフォローアップします。また植え込み型除細動器および心臓再同期療法後は遠隔モニタリングを導入し、致死的な不整脈の発生やデバイスのトラブルなどに速やかに対応できる体制をとっています。
本体の電池寿命は通常のペースメーカで5〜10年、リードレスペースメーカと植え込み型除細動器で5〜7年、心臓再同期療法は5年程度が目安となります。
現在使われているペースメーカは一定の条件を満たせばMRI検査を行うことができます。
施行にはいくつか条件がありますので診察時にお尋ね下さい。
ペースメーカをはじめとした植え込み型デバイスは高圧電流から生じる磁界の影響を受ける可能性があります。詳細は以下のサイトをご参照下さい。
http://www.jadia.or.jp/images/poster/wide/2011.pdf(日本不整脈デバイス工業会ホームページ)
また植え込み型除細動器の手術を受けた方は自動車運転を制限されることがあります。詳細は以下のサイトをご参照下さい。
http://new.jhrs.or.jp/public-site/activities04/pub-icd-crt/ (日本不整脈心電学会ホームページ)
診療実績
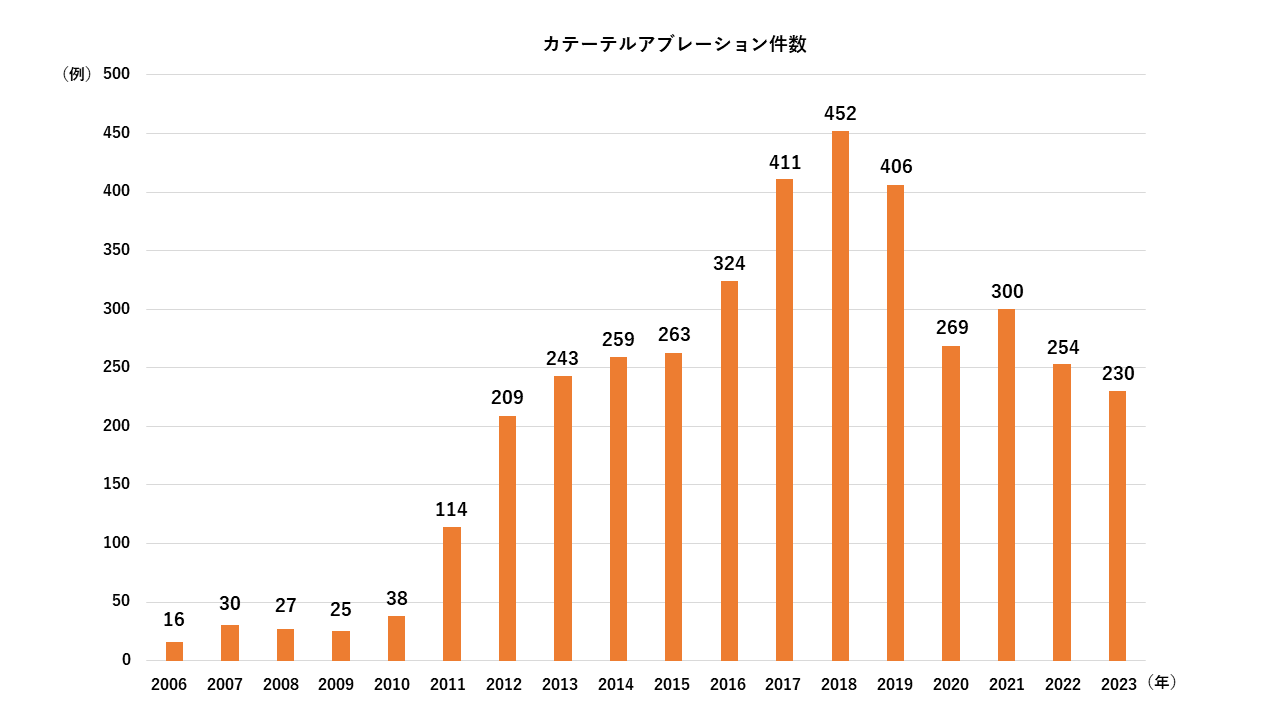
当院では年間200〜300件程度の手術が行われています。
(2016年から2019年は常勤医2名による手術件数、現在は1名で実施)
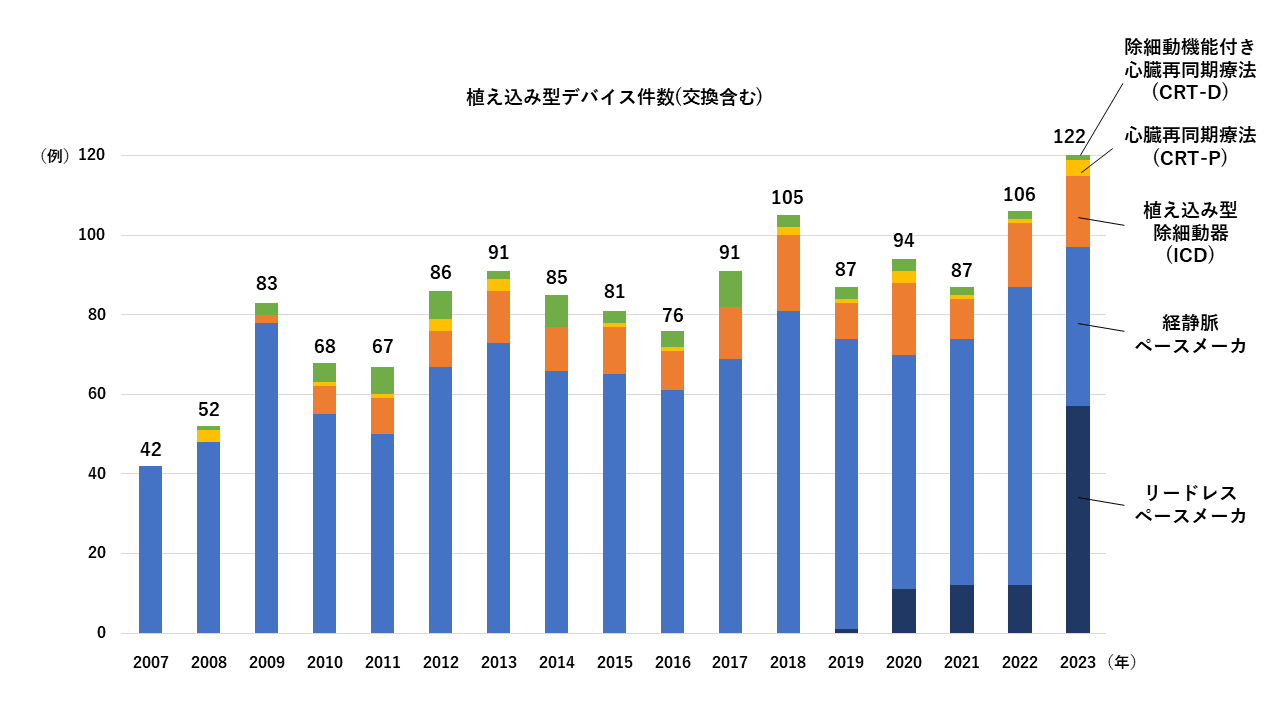
徐脈に対するペースメーカや致死性の頻脈に対する植え込み型除細動器(ICD)の手術、そして心不全に対する心臓再同期療法としてCRT-P/CRT-Dの植え込み手術を年間100件程度行なっています。(交換も含む)
医師紹介
 |
|
|||||
業績・論文(筆頭著者のみ)
第4回千葉大学循環器内科若手奨励賞 最優秀賞
第222回日本循環器学会関東甲信越地方会YIA最終選考
Ishimura M, Yoshimori A, Yamamoto M, Himi T, Kobayashi Y. Left atrial dual-loop reentry with endocardial and epicardial conduction pathway. HeartRhythm Case Rep. 2024 Sep 13;10(12):936-940. DOI: 10.1016/j.hrcr.2024.09.007☜(HeartRhythm Case Reportのサイトにリンクします。)
Ishimura M, Yamamoto M, Himi T, Kobayashi Y. Comparison of the effect of ethanol infusion into the vein of Marshall between with and without collateral veins. J Cardiovasc Electrophysiol. 2024 Jan;35(1):25-34. DOI: 10.1111/jce.16115.☜(Wiley Online Libraryのサイトにリンクします。)
Ishimura M, Yamamoto M, Himi T, Kobayashi Y. Efficacy and durability of posterior wall isolation with ethanol infusion into vein of Marshall. J Cardiovasc Electrophysiol. 2023;1-10. DOI: 10.1111/jce.15977☜(Wiley Online Libraryのサイトにリンクします。)
Ishimura M, Yamamoto K, Yamamoto M, Himi T, Kobayashi Y. Cardiac arrest due to late-onset coronary artery spasm after radiofrequency catheter ablation in a patient with an implantable cardioverter-defibrillator. Journal of Cardiology Case 2023 Feb;27(5):207-211 DOI:https://doi.org/10.1016/j.jccase.2023.02.006☜(Journal of Cardiology Casesのサイトにリンクします。)
Ishimura M, Yamamoto K, Yamamoto M, Himi Y, Kobayashi Y. Roof-dependent atrial flutter with epicardial conduction pathway masked by left atrium posterior wall debulking ablation. Ann Noninvasive Electrocardiol. 2022;00:e12997. DOI: 10.1111/anec.12997☜(Wiley Online Libraryのサイトにリンクします。)
Ishimura M, Yamamoto M, Himi Y, Kobayashi Y. Long‐term outcome of adenosine‐induced atrial fibrillation after atrial fibrillation ablation: A propensity score matching analysis. Pacing Clin Electrophysiol. 2022;1–8.DOI: 10.1111/pace.14557☜(Wiley Online Libraryのサイトにリンクします。)
Ishimura M, Yamamoto M, Himi T, Kobayashi Y. Durability of mitral isthmus ablation with and without ethanol infusion in the vein of Marshall. J Cardiovasc Electrophysiol. 2021 Aug;32(8):2116-2126. DOI: 10.1111/jce.15107☜(Wiley Online Libraryのサイトにリンクします。)
Ishimura M, Yamamoto M, Himi Y, Kobayashi Y. Real-time visualization of left inferior pulmonary vein isolation by ethanol infusion into the Marshall vein. Heart Rhythm. 2021 Feb;18(2):323-324. DOI: 10.1016/j.hrthm.2020.09.010☜(Heart Rhythmのサイトにリンクします。)
Ishimura M, Yamamoto M, Himi Y, Kobayashi Y. Atrial flutter with alternating tachycardia cycle length after atrial fibrillation ablation. HeartRhythm Case Rep. 2020 Oct 23;7(1):34-38. DOI: 10.1016/j.hrcr.2020.10.008☜(HeartRhythm Case Reportのサイトにリンクします。)
Ishimura M, Hama Y, Yamamoto M, Himi Y, Kobayashi Y. Infective endocarditis associated with recurrent cardiac tamponade after cardiac resynchronization therapy. HeartRhythm Case Rep. 2019 Jul 12;5(9):468-471. DOI: 10.1016/j.hrcr.2019.07.004☜(HeartRhythm Case Reportのサイトにリンクします。)
Ishimura M, Ueda M, Miyazawa K, Kajiyama T, Hashiguchi N, Nakano M, Kondo Y, Kanaeda T, Hiranuma Y, Kobayashi Y. Unexpected and unmanageable malfunctions of current co-radial pacemaker leads. Europace. 2015 Jan;17(1):166. DOI: 10.1093/europace/euu187☜(Europaceのサイトにリンクします。)
Ishimura M, Takayama M, Saji M, Takamisawa I, Umemura J, Sumiyoshi T, Tomoike H, Kobayashi Y. A case of hypertrophic obstructive cardiomyopathy with aortic stenosis. J Cardiol Cases. 2014 Jan 15;9(4):129-133. DOI: 10.1016/j.jccase.2013.12.003☜(Journal of Cardiology Casesのサイトにリンクします。)
外来受診・お問い合わせ
病院までのアクセスは病院ホームページをご参照下さい。
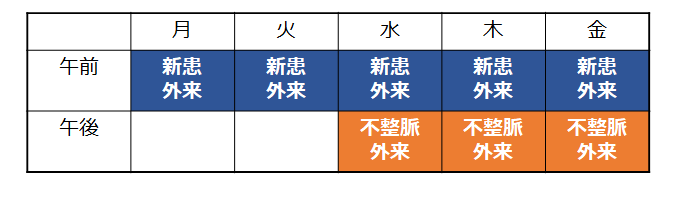
循環器の新患外来は月曜日〜金曜日の午前8時〜11時に受付しています。
不整脈外来は水曜日・木曜日・金曜日の午後になります。
紹介状のお持ちの患者さんは、患者総合支援センターへお問い合わせ下さい。
【問合せ先】君津中央病院(代表)0438-36-1071
【紹介予約専用電話】君津中央病院患者総合支援センター 0438-36-1069
2025年3月3日 更新